Bundan önceki yazılarda, termodinamiğin birinci yasası veya enerjinin korunumu ilkesi kapalı ve açık sistemlerle ilgili hal değişimleri hakkında bilgi vermiştik. Bu yazıda birçok kez vurgulandığı gibi, enerji var veya yok edilemez. Termodinamiğin birinci yasasına aykırı bir hal değişimi bugüne kadar görülmemiştir. Bu nedenle denilebilir ki, bir hal değişiminin gerçekleşebilmesi için birinci yasasının sağlanması zorunludur. Fakat aşağıda açıklandığı gibi, birinci yasanın sağlanması hal değişiminin gerçekleşebilmesi için yeterli değildir.
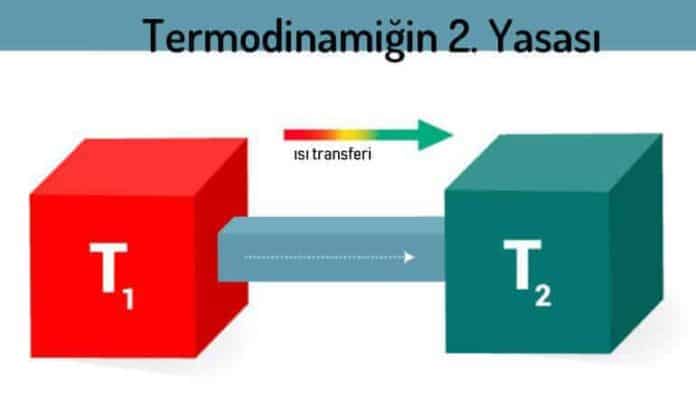
Masada bırakılan bir fincan sıcak kahvenin kısa sürede soğuduğu herkes tarafından bilinen bir olgudur. Fincan içindeki kahvenin hal değişimi termodinamiğin birinci yasasına uymaktadır, çünkü kahvenin yitirdiği enerji çevre havanın kazandığı enerjiye eşittir. Şimdi bunun tersi olan bir hal değişimini düşünelim: sıcak kahvenin çevre ortamdan alacağı enerjiyle ısınması. Böyle bir hal değişiminin olamayacağını biliyoruz, fakat gerçekleşseydi, havanın kaybettiği enerji kahvenin kazandığı enerjiye eşit olduğu sürece, birinci yasaya aykırı olmazdı.
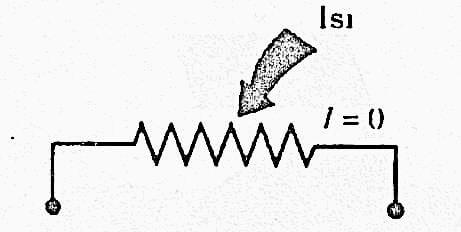
Bir başka örnek olarak, bir odanın elektrik direncinden geçen akımla ısıtılması göz önüne alınsın. Birinci yasaya göre direnç tellerine sağlanan elektrik enerjisi odaya ısı olarak geçen enerjiye eşit olmak zorundadır. Bu hal değişimini diğer yönde uygulayalım. Telleri ısıtarak tellerde eşit miktarda elektrik enerjisi sağlamak olanak dışıdır ve bu sonuç beklentilerimize uygundur. Fakat bu işlem yapılabilseydi birinci yasaya aykırı olmazdı.
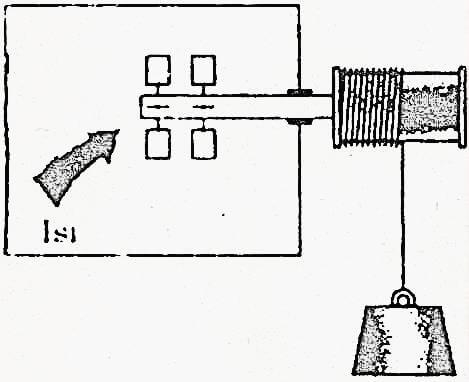
Son olarak bir kütlenin aşağı hareket etmesiyle çalışan karıştırma mekanizmasını ele alalım. Kütle aşağı inerken makara dönmekte ve makaraya bağlı döner kanat yalıtılmış kap içinde bulunan sıvıyı karıştırmaktadır. Sonuç olarak, kütlenin potansiyel enerjisi azalmakta, buna karşılık enerjinin korunumu ilkesine uygun olarak sıvının iç enerjisi artmaktadır. Fakat bunun tersi olan hal değişimi, başka bir deyişle sıvıdan döner kanata ısı geçişi sonucu kütlenin yükselmesi doğada karşılaşmayacağımız bir durumdur, oysa termodinamiğin birinci yasasına aykırı değildir.
Yukarıdaki örneklerden açıkça görüldüğü gibi, hal değişimleri belirli bir yönde gerçekleşirken, tersi olan yönde gerçekleşememektedir. Birinci yasa hal değişimlerinin yönü üzerinde herhangi bir kısıtlama koymaz, fakat birinci yasanın sağlanması hal değişiminin gerçekleşebileceği anlamına gelmez. Bir hal değişiminin olup olamayacağı konusunda birinci yasanın yetersizliği, bir başka genel ilkeyle, termodinamiğin ikinci yasasıyla kapatılır. Daha sonraki paragraflarda, yukarıda belirtilen ters hal değişimlerinin termodinamiğin ikinci yasasına aykırı oldukları gösterilecektir. Bu aykırılık, bir sonraki bölümde tanımlanacak olan entropi adlı özeliğin yardımıyla daha kolay belirlenecektir. Bir lıal değişimi termodinamiğin birinci ve ikinci yasalarını, sağlamıyorsa, gerçekleşemez (Şekil 5-5).
Termodinamiğin ikinci yasası değişik biçimlerde ifade edilebilir. Su anlatımlardan ikisi, termodinamik çevrim gerçekleştirerek çalışan mühendislik sistemleriyle ilgili olarak incelenecektir.
Termodinamiğin ikinci yasasının kullanımı sadece hal değişimlerinin yönünü belirlemekle sınırlı değildir, ikinci yasa enerjinin niceliği yanında niteliğini de ön plana çıkarır. Birinci yasa enerjinin niceliği üzerinde durur ve enerjinin bir biçimden diğerine dönüşümü sırasındaki değişimleri sayısal değerlerle ifade eder. Sayısal değer olarak eşit, fakat biçim ve kaynak bakımından farklı enerji arasında ayrım gözetmez. Enerjinin niteliğini korumak mühendislerin başlıca tasalarından biridir, ikinci yasa enerjinin niteliğini ve bir hal değişimi sırasında bu niteliğin nasıl azaldığını hesaplamak için somut yöntemler ortaya koyar. Bu bölümde daha sonra tartışılacağı gibi, yüksek sıcaklıkta enerjinin daha büyük bir bölümü işe dönüştürülebilir, bu nedenle aynı miktarda fakat düşük sıcaklıktaki enerjiye oranla niteliği daha yüksektir.
Termodinamiğin 2. yasası, ısı makineleri (motorlar) ve soğutma makineleri gibi temel mühendislik sistemlerinin verimlerinin üst veya kuramsal sınırını ve kimyasal reaksiyonların hangi oranda tamamlanacaklarını belirler.
Termodinamiğin ikinci yasasını açıklarken, ısıl enerji deposu adını vereceğimiz, yüksek ısıl enerji sığasına sahip, başka bir deyişle kütlesiyle özgül ısısının çarpımı çok yüksek olan cisimleri, sadece düşünce boyutunda da olsa tanımlamakta yarar vardır. Isıl enerji depolarından veya depolarına, depo sıcaklığı değişmeden sonsuz miktarda ısıl enerji geçişi olanaklıdır. Doğada da ısıl enerji deposu kavramını andıran örnekler vardır. Denizler, göller, akarsular ve çevremizdeki hava, çok büyük olan kütleleri nedeniyle birer ısıl enerji deposu olarak algılanabilir. Örneğin, kışın büyük bir kentin konutlarından olan ısı geçişi çevre havanın veya atmosferin sıcaklığını değiştirmez. Benzer biçimde, güç santrallerinde denizlere veya göllere verilen megajoule mertebelerindeki atık ısı, bu cisimlerin sıcaklıklarında bir değişikliğe yol açmaz.
iki fazlı bir sistem de bir bakıma ısıl enerji deposu olarak görülebilir, çünkü sabit sıcaklıktayken büyük miktarlarda ısıl enerji alır veya verir. Yakından bilinen bir başka örnek de endüstri kazanıdır. Kazan sıcaklıkları dikkatle kontrol edilir, böylece kazanlar büyük miktarlarda ısıl enerjiyi hemen hemen sabit sıcaklıkta sağlarlar. Bu bakımdan kazan bir ısıl enerji deposu olarak ele alınabilir.
Bir cismin ısıl enerji deposu kabul edilebilmesi için kütlesinin çok büyük olması gerekmez. Aldığı veya verdiği ısıl enerjiye oranla, ısıl enerji sığası büyük olan herhangi bir cisim ısıl enerji deposu olarak düşünülebilir. Örneğin, televizyondan çevreye olan ısı geçişini incelerken odadaki hava bir ısıl enerji deposu gibi ele alınabilir, çünkü televizyondan odaya geçen ısı, oda sıcaklığını duyulur ölçüde etkileyecek büyüklükte değildir.