Merhaba arkadaşlar bugün sizlere nükleer kararlılık, nükleer kararlılık eğrisi, nükleer kararlılığın kuralları, çekirdek spini ve spin manyetik moment anlatacağım. Çekirdeklerde, nötron ve protonların sıkı şekilde bir arada bulunmaları, şaşırtıcı gelebilir. Çünkü aynı cins yükler, (protonlar), özellikle, kısa mesafelerde birbirleri üzerine çok büyük itici elektrostatik kuvvetler uygularlar. Bu kuvvetler yüzünden çekirdeğin dağılması beklenir. Buna rağmen çekirdek dağılmaz, kararlıdır. Bunun nedeni, çekirdek kuvveti olarak adlandırılan başka bir kuvvetin var oluşudur. Bu kuvvet çok kısa menzillidir, (yaklaşık 2 fm). Çekici bir kuvvettir. Çekirdekteki tüm parçacıklara etki eder. Çekirdek kuvveti vasıtasıyla protonlar birbirini çekerler. Aynı zamanda Coulomb kuvveti nedeniyle de birbirini iterler. Çekirdek kuvveti, nötronlar arasında ve nötronlarla protonlar arasında da etkilidir.
Nükleer Kararlılık Eğrisi
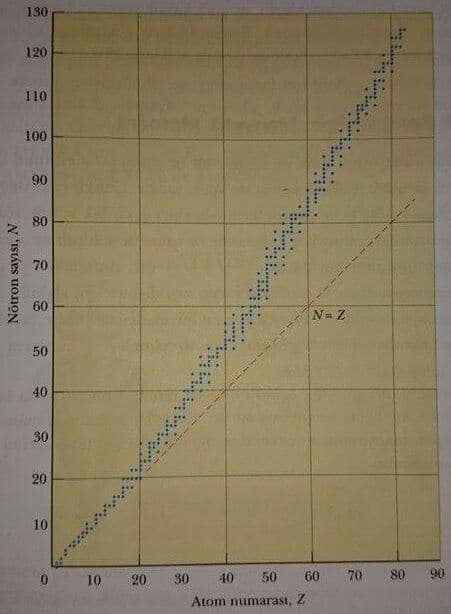
Yaklaşık 400 adet kararlı çekirdek vardır. Yüzlerce de kararsız çekirdek gözlenmiştir. Kararlı çekirdekler için N nin Z ye bağlı değişimi Şekil 1 de verilmiştir. Kararlı çekirdekler kararlılık çizgisi denen dar bir bölgede yer alan mavi noktalarla gösterilmiştir. Hafif çekirdekler eşit sayıda nötron ve proton içeriyorlarsa, yani N= Z ise daha kararlıdırlar. Ayrıca, Z= 20 üstünde, ağır çekirdeklerde ise nötron sayısı proton sayısına kıyasla daha büyükse bu çekirdekler daha kararlıdırlar. Bu durum aşağıdaki şekilde açıklanabilir. Protonların sayısı çoğaldıkça, Coulomb kuvvetinin şiddeti artar, çekirdeğin dağılmasına neden olur. Sonuç olarak, nötronlar sadece çekici kuvvete neden oldukları için çekirdeğin kararlı olması için daha çok sayıda nötrona gereksinim vardır. Bu dengeleme sınırsız değildir. Büyük Z değerleri için, protonlar arası itici kuvvet daha çok sayıda nötron ilavesiyle dengelenemez. Bu olay Z=83 değeri ile sınırlıdır. 83 den daha fazla proton içeren çekirdekler kararlı değildir.
Pek çok sayıdaki kararlı çekirdeğin A sayısının çift oluşu ilgi çekicidir. Dahası, Z ve N sayısının ikisinin birden tek sayı olduğu yalnızca sekiz çekirdek vardır. Gerçekte, N ve Z nin bazı değerleri için çekirdekler çok yüksek kararlılığa sahiptirler. N ve Z nin bu değerleri sihirli sayılar olarak isimlendirilirler. Bu sayılar
Z veya N= 2, 8 , 20 , 28 , 50 , 82 (44.2)
olarak bilinirler. Örneğin, alfa parçacıkları, (iki proton ve iki nötron) Z=2 ve N= 2, çok kararlıdır. Gittikçe artan büyük sihirli sayılara sahip çekirdeklerin görülmedik kararlığı, çekirdeklerin, atomik kabuk yapısına benzer bir kabuk yapısına sahip olduklarını gösterir.
Çekirdek Spini ve Spin Manyetik Moment
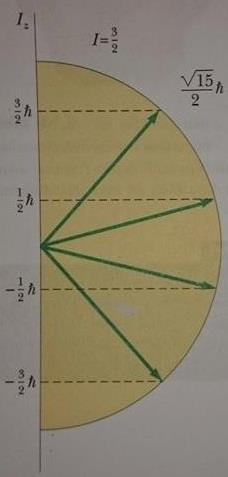
Çekirdeklerin de spini vardır. Çünkü çekirdeği oluşturan parçacıklar nötron ve protonların her biri çekirdek içinde yörüngesel açısal momentumları yanında 1/2 değerinde öz spine de sahiptirler. Çekirdeğin açısal momentumunun büyüklüğü ![]() dır. Buradaki I’ya çekirdek spin kuantum sayısı denir ve tam veya yarım sayı değerlerini alabilir. Spin açısal momentum vektörünün z bileşeninin en büyük değeri 1h dır. Şekil 2’de I=3/2, olması halinde çekirdek spininin olası yönelmeleri ve bunların Z ekseni üzerindeki bileşenleri verilmiştir.
dır. Buradaki I’ya çekirdek spin kuantum sayısı denir ve tam veya yarım sayı değerlerini alabilir. Spin açısal momentum vektörünün z bileşeninin en büyük değeri 1h dır. Şekil 2’de I=3/2, olması halinde çekirdek spininin olası yönelmeleri ve bunların Z ekseni üzerindeki bileşenleri verilmiştir.
Elektronlarda olduğu gibi, çekirdek açısal momentumunun da kendisine ait bir çekirdek manyetik momenti vardır. Bir çekirdeğin spin manyetik momenti, çekirdek manyetonu , μn cinsinden ölçülür. Bu moment birimi aşağıdaki şekilde tanımlanır.
Burada mp protonun kütlesidir. Bu tanım Bohr manyetonu μn tanımına benzer. Bohr manyetonu, serbest elektronun spin manyetik momentine karşılıktır. Proton ve elektronun kütleleri arasındaki fark nedeniyle , μn (= 9,274 x 10-24 J/T), μn den yaklaşık 2000 kere daha büyüktür.
Serbest protonun manyetik momenti 2,7928 μn’ye eşittir. Maalesef, bu değeri açıklayan çekirdek manyetizması ile ilgili genel bir teori yoktur. Diğer şaşırtıcı bir nokta, nötronun manyetik momentinin olmasıdır. Değeri -1,9135 μn dir. Eksi işareti momentin, spin açısal momentumunun zıt yönünde olması anlamındadır. Nötronun bir manyetik momente sahip bulunması, bunun bir temele dayanmadığını ancak daha çok belli bir yapıya sahip olduğunu ileri sürer.


