Merhaba arkadaşlar bugünkü yazımızda sizlere hidrokarbonlar, polimer hidrokarbonlar ve hidrokarbonların özelliklerini anlatacağız.Petrolde, doğal gazda, kömürde, birçok bitkinin özsuyunda, çiçeklerin, meyvelerin, baharatın aromasında bulunan hidrokarbonlar, günlük yaşamımızın ayrılmaz bir parçasıdır.
Petrolün arıtılması sırasında fiziksel – kimyasal yöntemlerle hazırlanan veya kimyasal yöntemlerle daha ayrıntılı bir şekilde dönüştürülen hidrokarbonlar, enerji ve birçok ürün (yağlayıcılar, deterjanlar, ilaçlar vb) verir. Belli başlı plastik maddeler, doğal kauçuk ve bunun gibi birçok sentetik elastomer aslında, binlerce, hatta milyonlarca kere zincirlenmiş özdeş motiflerden oluşan, dev hidrokarbon moleküllerinden başka bir şey değildir.
Gezegenimiz üzerinde bilinen ve işletilen bütün hidrokarbonlar biyogenetik kökenlidir. Bunlar, jeolojik katmanlar içinde hapsolmuş canlı organizma artıklarının, oksijensiz ortamda ve ısının etkisiyle uğradığı yavaş dönüşümler sonucunda oluşmuştur.
Hidrokarbonlar, yalnız Dünya gezegenine özgü değildir. Metan, Evren’in en önemli bileşenlerinden biridir; biyogenetik değil, kozmik kökenlidir, yani hidrojenin, termonükleer karbonla tepkimeye girmesinden kaynaklanmıştır. Metana yıldızlararası ortamda rastlanır; gaz, sıvı veya katı biçiminde, dev gezegenlerin Jüpiter, Satürn ve özelliklede, Uranüs ve Neptün bileşimine girer. Bu gezegenlerde ayrıca, güneş ışımasının yol açtığı foto-kimyasal tepkimelerden kaynaklanan daha ağır hidrokarbonların da varlığı bilinmektedir.
Hidrokarbon ‘ların Özellikleri
Moleküllerin çeşitliliği karbon – karbon ve karbon – hidrojen bağlarının birleşmesiyle oluşmuştur. Genel formülü CnH2n + 2 ve karbonlu zinciri dallanmamış olan alkanlar, C4 ’e kadar gaz, C5 ile C15 arasında sıvı ve bunun ötesinde katıdır. Bununla birlikte, zincirdeki dallanmalar, gaz haline dönüşmede bir artışa yol açar. Mesela, n-pentan 36 °C’de kaynar, oysa en dallanmış izomeri olan dimetil-2,2 propan ancak 9 °C’de kaynar. Suda hemen hemen çözünmez olan alkanlar (tıbbi parafin yağı gibi) tatsız ve kokusuzdur (algılanabilmesi ve dolayısıyla oluşturduğu tehlikenin farkına varılabilmesi için, kokulandırılması gereken metan gibi).
Alkanların kimyasal tepkinliği parafin adının çağrıştırdığı kadar zayıf değildir. Tam veya kısmı yükseltgenmenin yanı sıra, alkanlar kraking, halojenlenme, nitrolama tepkimelerine de girer. Bu arada, alkanların havanın oksijeniyle tepkimeye girmesinin uygulamada ve sanayide çok büyük bir önemi vardır; çünkü sözü edilen bu tepkime insanların tükettiği enerjinin en önemli bölümünü sağlamaktadır. Eğer alkanların yanması eksik bir şekilde yapılır veya buharla reforming yönteminde olduğu gibi su buharı eşliğinde gerçekleştirilirse, sentez gazı adı verilen çeşitli karbon ve hidrojen oksiti karışından elde edilir. Bu tepkime, gübreler için gerekli olan amonyağın üretiminde, metanol üretiminde ve daha başka birçok kimyasal tepkimede kullanılır.
Alkanların diğer iki tepkime türünün uygulamada büyük önemi vardır. Bunlardan ilki alkenleri ve sınaî organik kimyanın hemen bütün girdi ürünleri için gerekli aromatileri veren buharla kraking yöntemidir. Diğeri ise temel olarak aromatik hidrokarbonlar veren petrol arıtma işlemlerinden biri olan katalitik reforming yöntemidir. Bir hidrokarbon (etandan gazoile kadar) ve su buharı karışımı, çok kısa süreler (1 saniyeden daha az) için, yüksek sıcaklıklarda (8000C dolayında) tepkimeye sokularak, krakinge uğramış gazların birden soğutulmasıyla, en önemli bileşenleri alkenler olan (genel formülleri CnH2n) çeşitli karışımlar elde edilir: etilen, propilen, butenler, bu arada butadien ve aromatikler (benzen, tolüen, ksilen). Elde edilen bütün bu karışımların çeşitli yöntemlerle ayrılması, kimya sanayinde ham madde olarak kullanılacak olan alkenlerin ve aromatiklerin saf olarak elde edilmesine olanak sağlar. Alkenler veya olefinler, büyük kimyasal tepkinlik özellikleri nedeniyle yaygın olarak kullanılan maddelerdir. En basit iki alken çeşidi olan etilen (eten) ve propilen (propen), aynı zamanda uygulamada en çok kullanılanlardır. Alkanların buharla kraking yöntemiyle işlendiği birimlerde milyonlarca ton düzeyinde üretilen alkenler, birçok kimyasal tepkimeye yatkındır.
Nitekim etilen, polietilen halinde polimerleşebilir, vinil klorüre veya stirene dönüştürülebilir, sonradan etilen – glikole, gerilimetkin maddelere ve başka ürünlere dönüştürülmek üzere, etanole veya etilen okside de yükseltgenebilir. Propilene gelince, çok sayıda polimer verir: polipropilen (otomobil sanayinde en çok kullanılan hidrokarbonlardan biridir), poli-akrilonitril (mesela akrilik iplik yapımı için), poliüretanlar için polioller (yalıtkan köpükler), boyalara ve mürekkeplere yönelik reçineler için akrilatlar vb. Propilen ayrıca, birçok başka sanayi ürününün sentezinde hammadde olarak da kullanılır: hayvan yemi olarak kullanılan aminoasit çeşidi olan metiyonin veya fenol üretiminde kullanılan aromatik bir hidrokarbon olan kümen gibi.
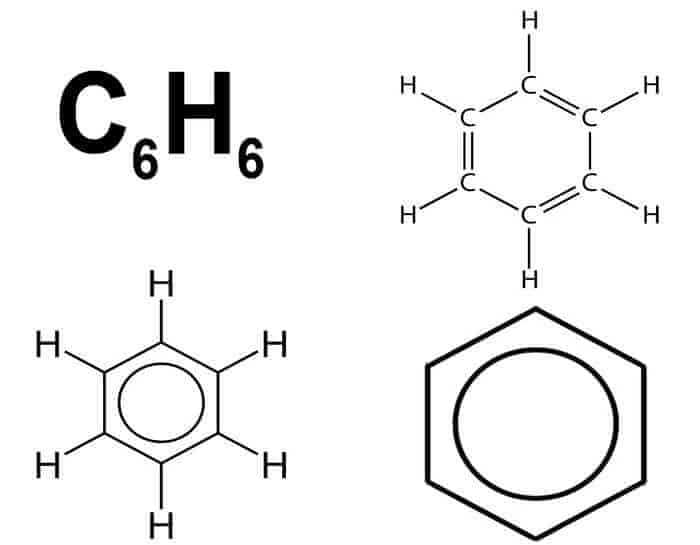 Aromatikler, altı karbon atomlu bir veya daha çok benzen halkası içeren hidrokarbonlar olarak tanımlanır. Düzlemsel olan yapılan nedeniyle, aromatikler dediğimiz bu hidrokarbonların bağ enerjileri özellikle çok yüksektir. Bir örnek olarak benzeni (C6H6)ele aldığımızı düşünelim; benzende, rezonans enerjisi denen bu fazla enerji eşlenik çift bağların elektronlarının yöresizliğinden kaynaklanmaktadır. Bunun sonucunda, çok ilgi çekici kimyasal özellikler ortaya çıkar; özellikle aromatik halkanın hidrojen atomlarını, çok sayıda işlevsel grupla onartma imkanı doğar. Benzenin bu özelliği, bunun, son derece çeşitlilik gösteren kimyasal ürünlerin elde edilmesinde kullanılmasına imkân verir: polimerler, çeşitli ilaçlar, boyar maddeler.
Aromatikler, altı karbon atomlu bir veya daha çok benzen halkası içeren hidrokarbonlar olarak tanımlanır. Düzlemsel olan yapılan nedeniyle, aromatikler dediğimiz bu hidrokarbonların bağ enerjileri özellikle çok yüksektir. Bir örnek olarak benzeni (C6H6)ele aldığımızı düşünelim; benzende, rezonans enerjisi denen bu fazla enerji eşlenik çift bağların elektronlarının yöresizliğinden kaynaklanmaktadır. Bunun sonucunda, çok ilgi çekici kimyasal özellikler ortaya çıkar; özellikle aromatik halkanın hidrojen atomlarını, çok sayıda işlevsel grupla onartma imkanı doğar. Benzenin bu özelliği, bunun, son derece çeşitlilik gösteren kimyasal ürünlerin elde edilmesinde kullanılmasına imkân verir: polimerler, çeşitli ilaçlar, boyar maddeler.
Polimer Hidrokarbonlar
Bir çift bağa sahip olan alkenler, kendi kendiyle veya aynı aileden alkenlerle tepkimeye girerek polimerler veya kopolimerler (eşpolimerler) vermeye çok yatkındır. Bu dev moleküller, sanayinin bir ürünüdür; çünkü kauçuk ve birkaç bitkisel reçine dışında, yüksek molekül kütleli doğal polimer hidrokarbonlara bugüne kadar rastlanmamıştır.
Etilenin polimerleştirilme tepkimesi, 1930 yılında, tesadüf eseri olarak İngiliz kimyasal ürünler şirketi İmperial Chemical İndustries’de bulundu. Ama başlangıçta, yaklaşık 2000 barlık çok yüksek basınçlar altında gerçekleştirilen bu tepkimenin teknolojisini kolayca uygulanabilir hale getirmek için yıllar gerekti. Çok geçmeden ilginç mekanik ve elektriksel özelliklerinin farkına varılan polietilen, birçok farklı uygulamada kullanılmaya başladı. Daha sonra, 1950’li yıllarda kimyacı K. Ziegler, düşük basınç altında (100 bardan daha az) polimerleştirme tepkimesini geliştirdi. Bu yöntem 1970’li yıllarda polietilenin bütün çeşitlerine yaygınlaştırıldı; böylece o tarihten itibaren polietilen, dünya çapında en çok kullanılan plastik madde haline geldi. Çöp torbasından elektriksel yalıtıma kadar uzanan çok çeşitli alanlarda kullanıldı.
Propilenin polimerleştirilmesiyse ancak birkaç yıl sonra, birçok kuramsal ve teknik ilerlemenin ardından başarılmıştır. Gerçekte, propilen monomerlerinin uzayda zincirlenmesi için üç yol vardır; ama bunlardan ancak biri, yanı izotaktik polimerleşme, ilginç mekanik özellikleri olan dev moleküller verir. Günümüzde polipropilen, kondansatörler için gerekli olan çok ince filmden bahçe mobilyalarına kadar çok sayıda kullanım alanı bulmuş olan plastik maddelerden biridir.

Hidrokarbonlardan türemiş olan üçüncü büyük plastik madde polistirendir; bu madde, aromatik bir halka içeren bir alken olan stirenin polimerleştirilmesi yoluyla elde edilir; stiren ise, etilenin benzenle olan bir tepkimesi sonucunda elde edilen bir maddedir. Stiren kütlesel olarak veya sulu asiltı halinde kolaylıkla polimerleşebilir. Ayrıca, çift bağ taşıyan çok sayıda bileşikle kopolimerleşme özelliği de vardır. Bu büyük kopolimerler ailesinin, çok çeşitli uygulama alanları vardır.
Doğal kauçuğun ve çeşitli elastomerlerin de eklenmesi gereken bu üç büyükten başka, kimyacılar, yüksek molekül kütleli ve hidrokarbon yapılı başka plastik maddeleri ve reçineleri de sentezleyebilmektedir.


